安科生物参股公司元宋生物新增针对复发脑胶质瘤中国临床试验注册批件
发布日期:2026-03-26 浏览次数:1321
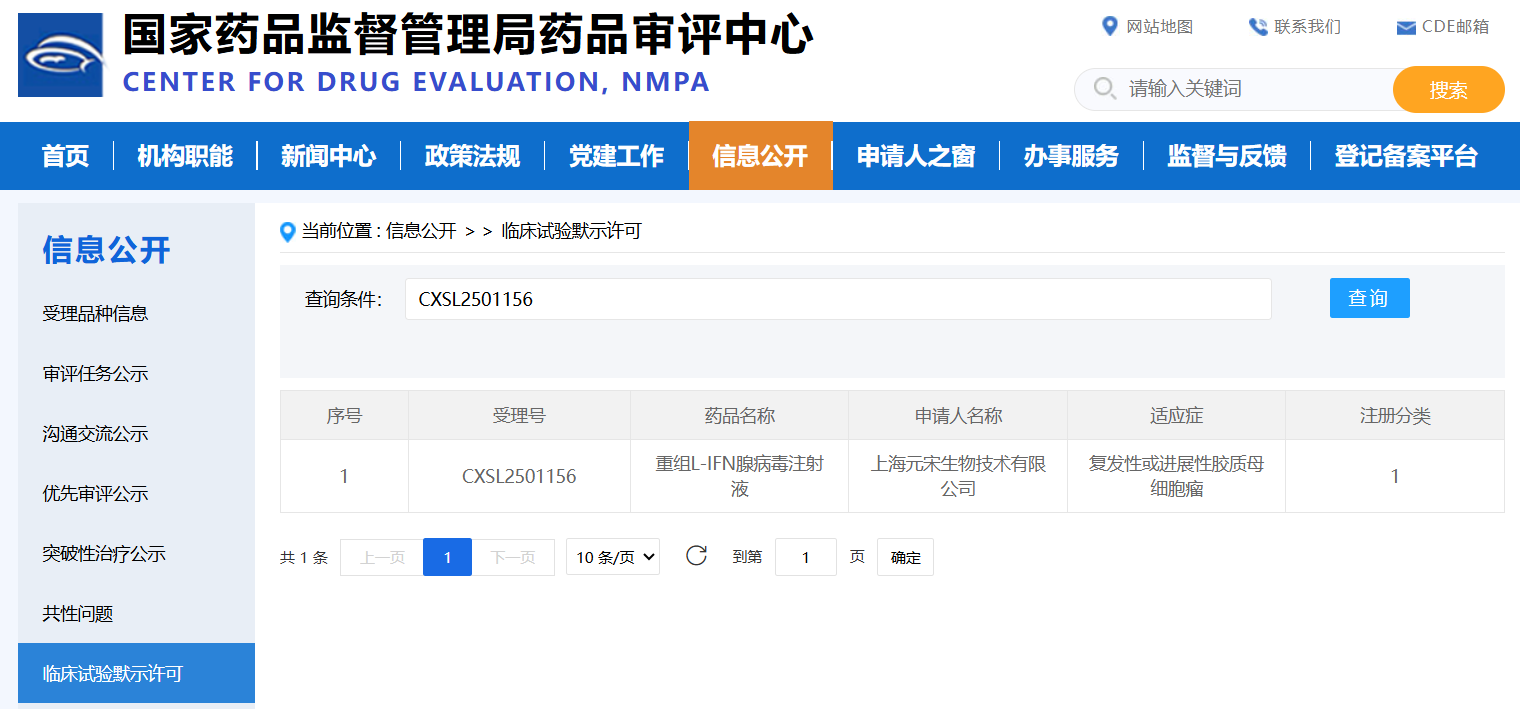
安科生物参股公司上海元宋生物技术有限公司宣布,其自主研发的一类抗癌新药——重组L-IFN腺病毒注射液(YSCH-01)于2026年3月25日收到国家药品监督管理局药品审评中心(CDE)签发的药物临床试验批准通知书,获批开展针对复发性或进展性胶质母细胞瘤(GBM)的注册临床研究。
胶质母细胞瘤(GBM)是恶性程度极高的脑肿瘤,术后复发概率接近100%。复发后患者中位生存期仅约5.9个月,一年生存率不到15%。当前胶质母细胞瘤标准治疗方案效果有限,现阶段缺乏高效的后线治疗方案,临床迫切需要创新且有效的治疗方法。
重组L-IFN腺病毒注射液(YSCH-01)是元宋生物基于“癌症的靶向基因-病毒治疗(CTGVT)”平台自主研发的重组溶瘤腺病毒产品,采用肿瘤靶向双调控的溶瘤腺病毒技术,实现肿瘤组织选择性杀伤的同时保证安全性,该产品还携带类干扰素样重组抗癌基因,能够显著增强抗肿瘤免疫反应。
这是YSCH-01在GBM适应症上取得的又一重要进展。此前,本产品先后于2023年12月、2024年4月获得美国FDA和中国CDE临床试验许可,用于治疗晚期实体瘤;并于2025年12月获得美国FDA批准,新增复发GBM适应症。此次国内注册临床研究的获批,标志着YSCH-01在中美两地同步推进GBM这一核心适应症的开发,进一步拓展了该产品在肿瘤治疗领域的临床研究布局。
元宋生物CEO章康健博士表示:“YSCH-01在复发GBM适应症上获得CDE注册临床批件,是产品开发战略的又一重要里程碑。基于前期研究展现出的卓越潜力和安全性,我们相信YSCH-01有望为国内GBM患者提供新的治疗选择。我们将迅速推进临床研究,加速这一创新疗法的开发进程。”

安科生物参股公司上海元宋生物技术有限公司宣布,其自主研发的一类抗癌新药——重组L-IFN腺病毒注射液(YSCH-01)于2026年3月25日收到国家药品监督管理局药品审评中心(CDE)签发的药物临床试验批准通知书,获批开展针对复发性或进展性胶质母细胞瘤(GBM)的注册临床研究。
胶质母细胞瘤(GBM)是恶性程度极高的脑肿瘤,术后复发概率接近100%。复发后患者中位生存期仅约5.9个月,一年生存率不到15%。当前胶质母细胞瘤标准治疗方案效果有限,现阶段缺乏高效的后线治疗方案,临床迫切需要创新且有效的治疗方法。
重组L-IFN腺病毒注射液(YSCH-01)是元宋生物基于“癌症的靶向基因-病毒治疗(CTGVT)”平台自主研发的重组溶瘤腺病毒产品,采用肿瘤靶向双调控的溶瘤腺病毒技术,实现肿瘤组织选择性杀伤的同时保证安全性,该产品还携带类干扰素样重组抗癌基因,能够显著增强抗肿瘤免疫反应。
这是YSCH-01在GBM适应症上取得的又一重要进展。此前,本产品先后于2023年12月、2024年4月获得美国FDA和中国CDE临床试验许可,用于治疗晚期实体瘤;并于2025年12月获得美国FDA批准,新增复发GBM适应症。此次国内注册临床研究的获批,标志着YSCH-01在中美两地同步推进GBM这一核心适应症的开发,进一步拓展了该产品在肿瘤治疗领域的临床研究布局。
元宋生物CEO章康健博士表示:“YSCH-01在复发GBM适应症上获得CDE注册临床批件,是产品开发战略的又一重要里程碑。基于前期研究展现出的卓越潜力和安全性,我们相信YSCH-01有望为国内GBM患者提供新的治疗选择。我们将迅速推进临床研究,加速这一创新疗法的开发进程。”
















